
2. フォローアップSPECTを再考する
座長
沖崎 貴琢 先生
旭川医科大学
石井 秀樹 先生
群馬大学
演者
坂谷 知彦 先生
大阪鉄道病院
本講演では、フォローアップSPECTを「PCI、CABGなど血行再建術後、おおよそ1年以内に実施される心筋SPECT」と定義する。
現時点における本邦での心筋SPE C Tの位置づけとして、「慢性冠動脈疾患診断ガイドライン(2018年改訂版)」では「冠動脈血行再建術の適応を決定する場合」や「心筋梗塞の部位診断を行う場合」のエビデンスレベルは推奨クラスⅠとされている1)。一方で「PCI後2年以内のルーチン検査」に関してはクラスⅢであり、推奨されていない。その根拠の一つとして、高リスクPCIを受けた患者1,706例を1年後にルーチンの負荷検査を受ける群と通常のケアを行う群で無作為に割り付けて比較した研究結果がある。同研究では、両群において2年後の臨床転帰に有意差はなかったと報告されている2)。
一方、COURAGE試験のサブ解析では、治療により5%以上の虚血改善が得られた群は予後良好であったとされている3)。
同様に本邦のJ-ACCESS4試験においても、虚血改善が5%未満にとどまった群では5%以上の改善群に比べ予後が悪いことや、残存虚血が認められた群では予後不良であることを示すデータが得られている4)。これらの知見から、血行再建後の予後不良リスクが高い患者を適切に抽出するために心筋SPECTは有用といえる。
フォローアップSPECT実施の意義について私見をまとめると以下のようになる。
- 1.虚血の改善が得られているかどうか(特に多枝病変で過小評価が疑われる場合)
- 2.高リスク患者の予後が改善できたかどうか(特にISCHEMIA試験の除外例)
心筋SPECTは基本的に相対的表示であるため、特に多枝病変では病変枝が偽陰性となる可能性がある。そのため、虚血の過小評価が疑われる症例に対しては、血行再建後に残存虚血を評価することが必要な場合がある。
ISCHEMIA試験では、負荷により中等度以上の虚血が誘発された患者であっても、保存的治療戦略に対する血行再建の有用性は示されなかった5)。しかし、同試験では腎機能障害や重度の狭心症、急性冠症候群(ACS : acute coronary syndrome)、左室機能不全、心不全などの疾患群が除外されている。この除外基準に合致する患者の予後は悪いことが確認されており6)、高リスク患者では血行再建後も慎重な管理が求められる。
SPECTの自験例
- ■症例 70代男性 労作性狭心症
約30年前に左前下行枝(LAD)にベアメタルステント留置
長らく経過良好であり、10年前の心筋SPECTでは集積低下を認めなかった。薬物治療を継続していたが、心エコー図で左室下壁の壁運動異常を認めたため、半年前に心筋SPECTの再検査を実施した。負荷時像、安静時像共に壁運動異常の領域に一致して高度集積低下を認め、左室下壁の心筋障害が示唆された。また、左室前壁中隔にも軽度の集積低下がみられた(図1)。

【図1】
こうした新たな所見を踏まえ、10年ぶりに冠動脈造影(CAG : coronary angiography)を施行した。すると、右冠動脈(RCA)は右室枝(RV branch)の分岐部で完全閉塞しており、順行性の血流はほとんど認められなかった(図2上)。左冠動脈(LCA)に関しては、左回旋枝(LCx)末梢に狭窄があり、左前下行枝(LAD)にもびまん性に狭窄を認めた(図2下)。
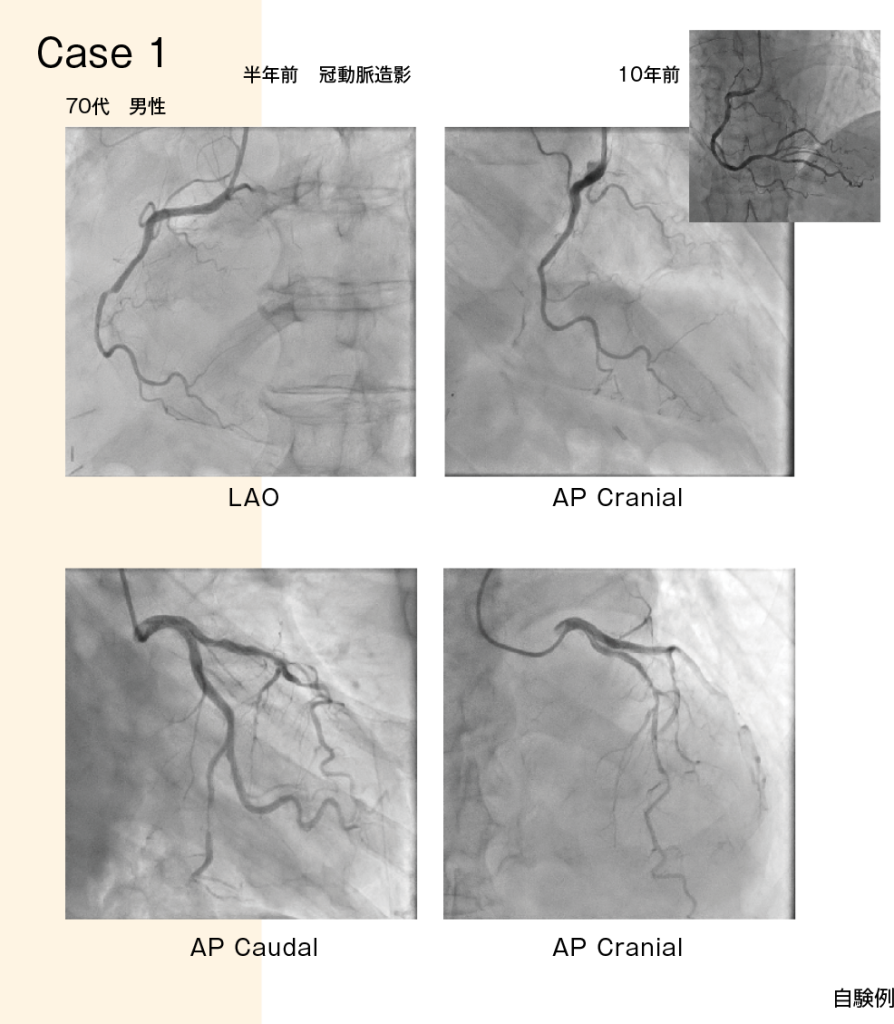
【図2】
LADからRCAへgrade1程度の側副血行路を認めた。RCAの完全閉塞を含む3枝病変であり冠動脈バイパス術(CABG)も考慮されたが、併存疾患により日常生活動作(ADL)も低下していることから、患者・家族との共同意思決定(SDM : shared decision making)によりPCIが選択された。標準的にはRCAにPCIを行うが、RCAの完全閉塞距離が長いため、LCxとLADに対し血行再建を行った。
PCI施行後、RCAの閉塞による影響を判定するためフォローアップSPECTを実施した。負荷時像では、下壁で若干の集積低下を認めたが、高度虚血ではないと判断した。また、LAD・LCx領域でも虚血の誘発は認められなかった(図3)。
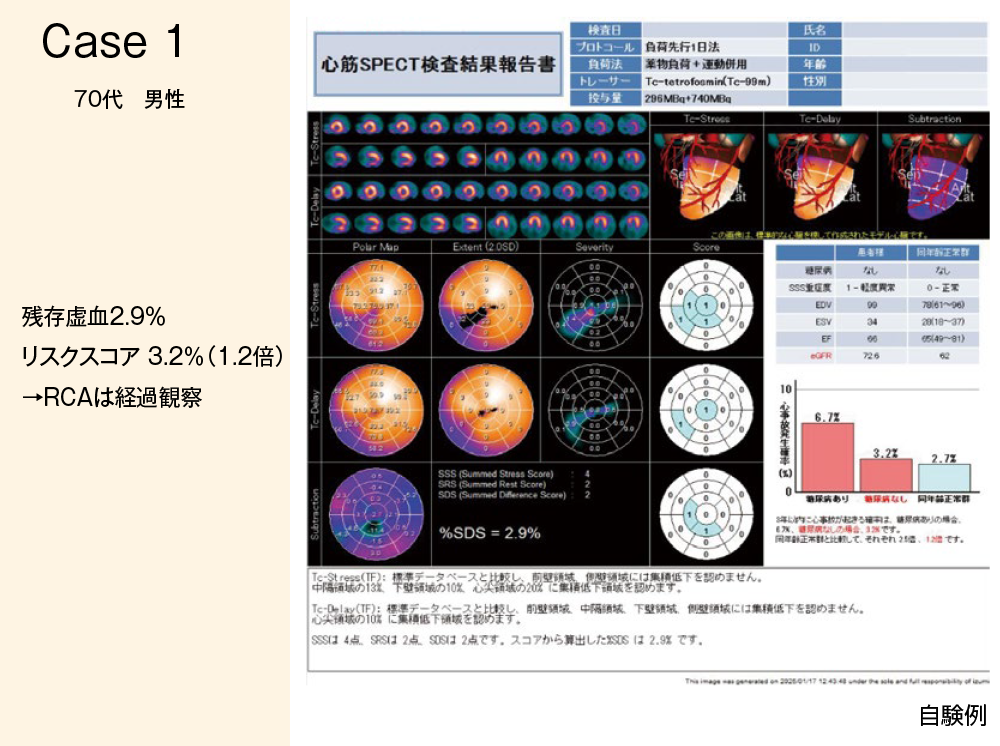
【図3】
Heart Risk View-S(HRV-S)を用いた解析(図3右)では、虚血心筋量は約3%、リスクスコアは3.2%で同年代正常人と比較して1.2倍と低値であった。さらに、LVEFは66%とglobal functionも保たれていることから、本症例は薬物療法継続とした。
Heart Risk View-S(HRV-S)は、心筋SPECTから得られる情報を基に、糖尿病の有無等のリスク因子を加味して心事故発生確率を自動算出するソフトウェアである。一般的に、心筋SPECTが正常であれば予後は良いと考えられる。ただし、我々が心筋SPECT正常[SSS(summed stress score)≦3]の698例を追跡調査したところ、3.8年±2.4年の観察期間中に21例(3.0%)の心事故を確認している7)。HRV-Sで算出した心事故発生確率は、心事故群が非心事故群に比べて有意に高かった(5.5±2.6 vs 2.9±2.6%、カイ二乗検定 p<0.001)。心事故発生確率のカットオフ値を3.4%に設定すると、2群間で有意差が認められた(感度76%、特異度72%、AUC 0.85)。
以上の知見を基に、虚血性心疾患の治療方針について提唱した内容8)を図4に示す。

【図4】
心筋SPECTで5%以上の虚血心筋量を認める場合は血行再建が推奨される。また、虚血心筋量が5%未満で、SSSが低値であっても、HRV-Sよる心事故発生確率が3.4%以上であれば、心筋SPECT偽陰性の除外のためにCAGを検討すべきと考える。
高リスク患者におけるルーチンのフォローアップSPECTには否定的な報告もあるが、SPECT陰性例では心事故発生率は1%/年未満とされており9)、HRV-Sと組み合わせることで、より詳細なリスク判定が可能となるだろう。