
2. AIによる心筋SPECT診断の進化と定量評価の可能性
座長
松本 直也 先生
日本大学
福島 賢慈 先生
福島県立医科大学
演者
鈴木 康之 先生
日本大学
本学では、2020年から負荷心筋SPECT向けAI自動診断支援システムの開発プロジェクトをスタートさせ、その歩みを進めている。開発プロジェクトの前提となる心筋SPECTの定量評価の価値を振り返るとともに、本学での検討を中心に心臓核医学分野におけるAI診断開発の現状について解説する。
心筋SPECT検査では、虚血の有無だけでなく、虚血心筋量や責任冠動脈、心機能回復の可能性など広範な情報を入手することが可能である。こうした情報を基に治療選択の判断に加え、治療後の予後予測に資する情報も得ることができる。この点については、血行再建による虚血改善度により予後の差が生じること1)、さらに虚血減少5%以上の達成が予後に大きく影響することが我々の研究でも示されている1)。また心筋SPECTでは、虚血心筋量の視覚的半定量スコアとしてSSS(summed stress score)などが用いられており、この指標を用いたリスク層別化能は国内外の大規模の臨床研究により証明されている2)3)。
その一方で、心筋SPECTの課題として、読影に一定程度の熟練を要することや、多枝病変や主幹部病変などの重症冠動脈疾患において偽陰性を生じやすいことが知られている。また、本邦では心筋SPECTについて高い精度と再現性を持って読影が可能な専門家が充足しているとは言えない実情もあり、この点が臨床における課題の一つとなっている。
こうした課題に対応し、視覚読影熟練者を必要とするSSSを代替する定量指標として、自動定量が可能なTPD(total perfusion deficit)4)が評価に用いられることがある。
また、心筋SPECTによる心電図同期撮影時のデータも重要である。これにより得られる左室駆出率(LVEF : left ventricular ejection fraction)や拡張末期容積(EDV : end diastolic volume)は、心イベント予測に重要な指標となり、負荷時と安静時のEDVの比をとるTID(transient ischemic dilatation)ratioは、SSSやTPDで見落とされやすい重症冠動脈病変や多枝冠動脈病変の検出に役立つ。さらに、心電図同期撮影データからは、心筋の各セグメントの同期性を評価する左室位相解析指標の位相バンド幅(BW : bandwidth)、標準偏差(SD : standard deviation)、Entropyという3種のユニークかつ有用な指標も得られ、TPDやLVEFと併せて検討することで、高い予後予測能を有することが報告されている5)6)。
前述のようにこれまでの研究により、心筋SPECTをベースにした様々な有用な指標が見出されてきた。しかし、それらの指標はわずかな変数間の直接的な関係を記述する伝統的な統計モデルに基づき見出されたものであり、実臨床における多様かつ複雑な臨床情報や検査結果情報の数々を統合して検討することは難しかった。
そこで現在、世界各国で進められているのがAI、機械学習・ディープラーニングの技術を用いた診断支援システムの開発である。ディープラーニングの技法は、入力した情報の特徴量の抽出と情報量圧縮を繰り返しながら、得られた特徴量を元にした分類や予測を行う方法であり、多変量のデータから学習した特徴量の関連性に基づくアウトプットを得られる特徴がある。
例えば冠動脈疾患領域では、AI診断開発で先行する米国Cedars-Sinai Medical Centerが図1のようなディープラーニングモデル診断システムを設計している。
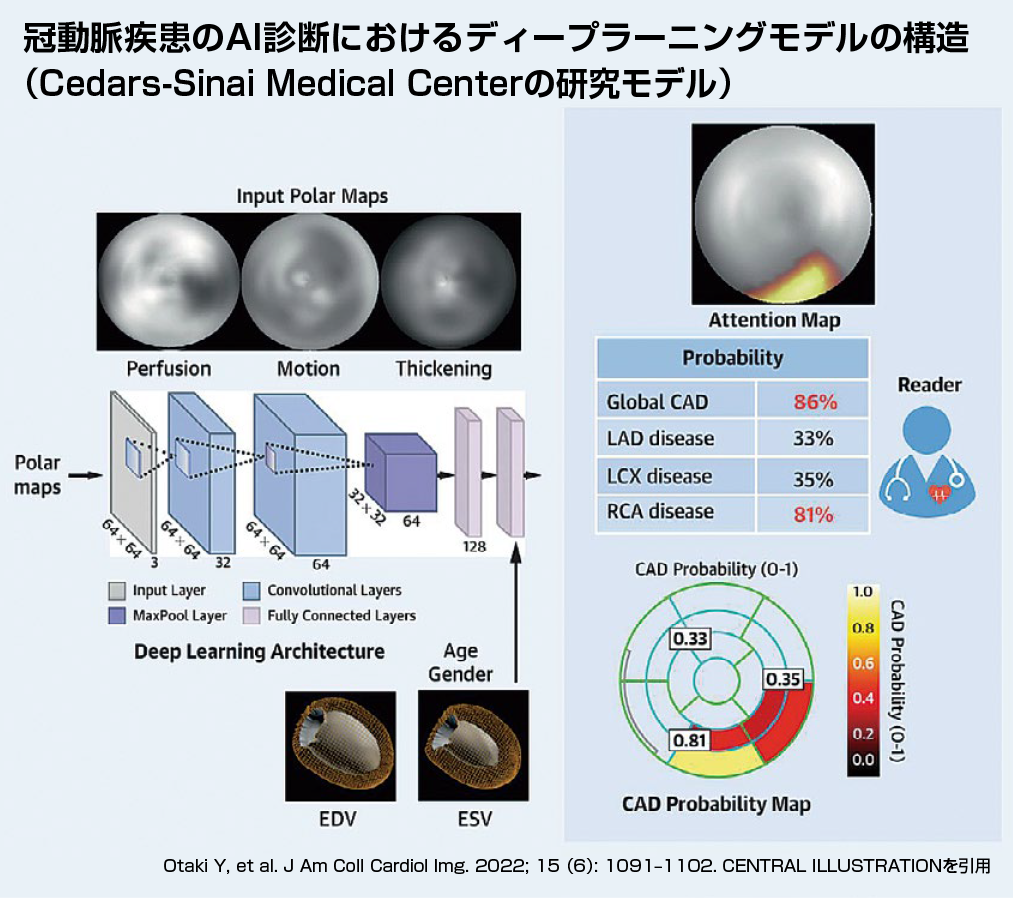
【図1】
血流、壁運動、収縮時壁肥厚率のPolar Map情報と年齢、性別、そしてEDV、収縮末期容積(ESV : end systolic volume)の情報を加えたモデルである7)。冠動脈疾患の診断能はAUC(area under the curve)0.83であり、人間による診断能(TPDを用いた虚血心筋量による評価 同0.78、専門医の診断 同0.71)より有意に診断能を改善したと報告されている(Wilcoxonの順位和検定、p<0.0001)7)。
ここからは本学における実践を紹介する。
本学独自のAIモデル開発の課題解決目標は以下の3つである。
- 心筋SPECTにおける専門医レベルのAI診断
- 専門医を介在しない診断=診断の自動化
- 可能ならば、専門医を超える診断能を実現したい
2024年の米国心臓核医学会(ASNC)で報告した本学で開発中のディープラーニングを用いたアルゴリズムによるAIモデルの多枝病変の診断に関する診断能の検証結果を供覧する。
AIモデルの入力情報は、本稿前半で紹介した心筋SPECTによる定量情報が主体であり、TPD、LVEF、EDV、TID ratioに加え、位相解析のパラメータであるBW、SD、Entropyなどを採用している(図2)。
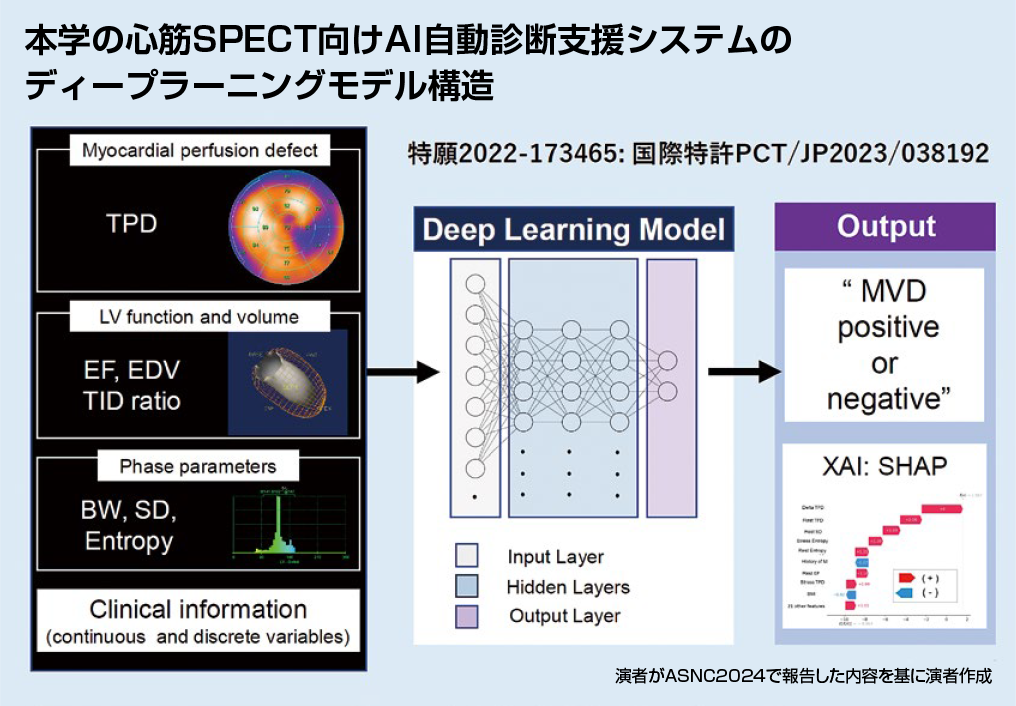
【図2】
さらに、様々な臨床情報や心電図などの検査結果などを加えた50以上のパラメータを入力情報、学習情報として使用した。
AI活用の大きな論点として、結果が示されてもその評価の背景や判断根拠を明確に説明できないブラックボックス化の問題が指摘されている。参照した各特徴量の重要度を数値化して示すSHAP(SHapley Additive ex Planations)valueと呼ばれる指標を用いて、説明可能AI(XAI:explainable AI)の手法により結果の背景説明を一定程度可能にしている。
実際の症例約1,000件のデータを用いて訓練し、学習データとは異なる200例を用いてシステムの診断精度を検証した。本システムの多枝病変の診断能は、AUCで0.88±0.03であり、それぞれ単独で診断した場合のStress TPD 0.82±0.03やTID ratio 0.50±0.12に対して有意な改善を認めた(p<0.05)。なおSSS単独では同0.84±0.06、SDS単独では同0.88±0.07であった。もちろん現在の臨床でTPD単独で診断することは想定されないため、医師による心筋SPECTの読影による診断を対照とした診断能の検討も現在進めており、十分な精度を有することが示されてきている。
AIによる診断根拠については、深層学習モデルによる特徴量の重要度SHAP valueで上位10項目をみると、Ischemic TPD(ΔTPD:負荷時と安静時のTPDの差)、LVEF、EDV、TID ratio、位相解析指標のパラメータであるEntropyやBWなどのデータが重視され、解が導き出されたことが分かっている。
今後のシステム開発では、対象症例を拡大するとともに、数値情報だけではなく、画像情報とのコンビネーションを図るマルチモーダル対応の準備を進めている。併せて、社会実装に向けた医療AI診断システムの倫理的側面への配慮や安全性、情報セキュリティの課題にも取り組み、心臓核医学のAI開発が本格化する時代の良き先例となることを目指したい。
AI診断支援システムのデモ症例 80代男性 心筋梗塞の既往あり
心筋SPECTにおいてLAD領域の欠損と、下壁領域の可逆性を有する血流欠損を認める明らかな多枝病変様を呈するケースである。位相解析による負荷時のBWも102と安静時に対して拡大し、Entropyについても負荷時61.5と安静時よりも増大していた(図3)。
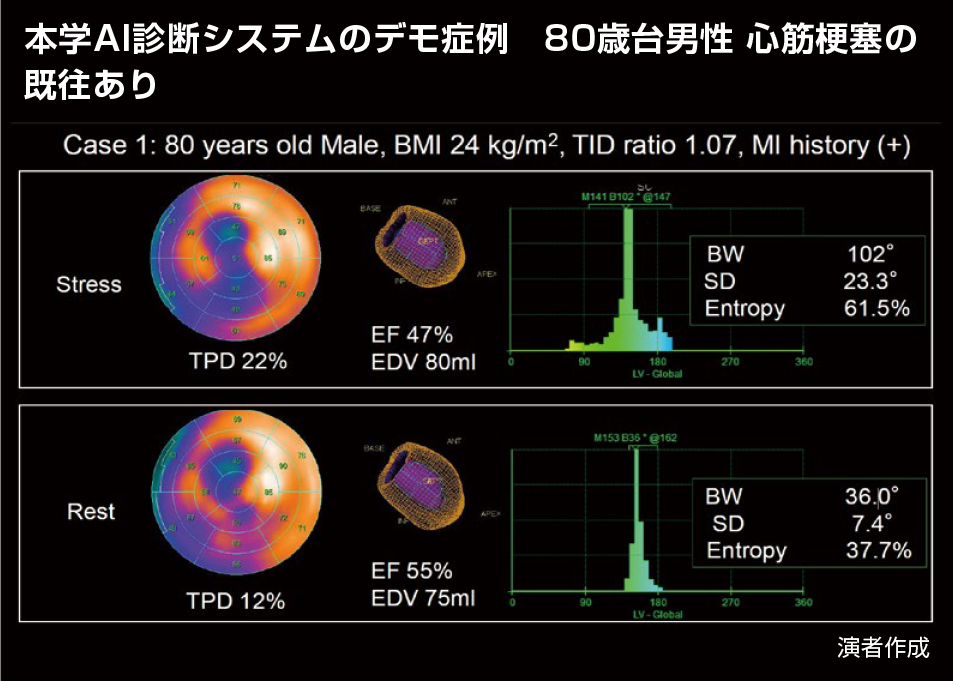
【図3】
AIモデルによる自動診断では、多枝病変陽性と結果が示された。SHAP valueを用いたXAIの診断根拠の提示では、図4のWater fall plot法による横棒グラフの通り、TPDやEntropy、LVEFなどを根拠に陽性としたことが示されている。
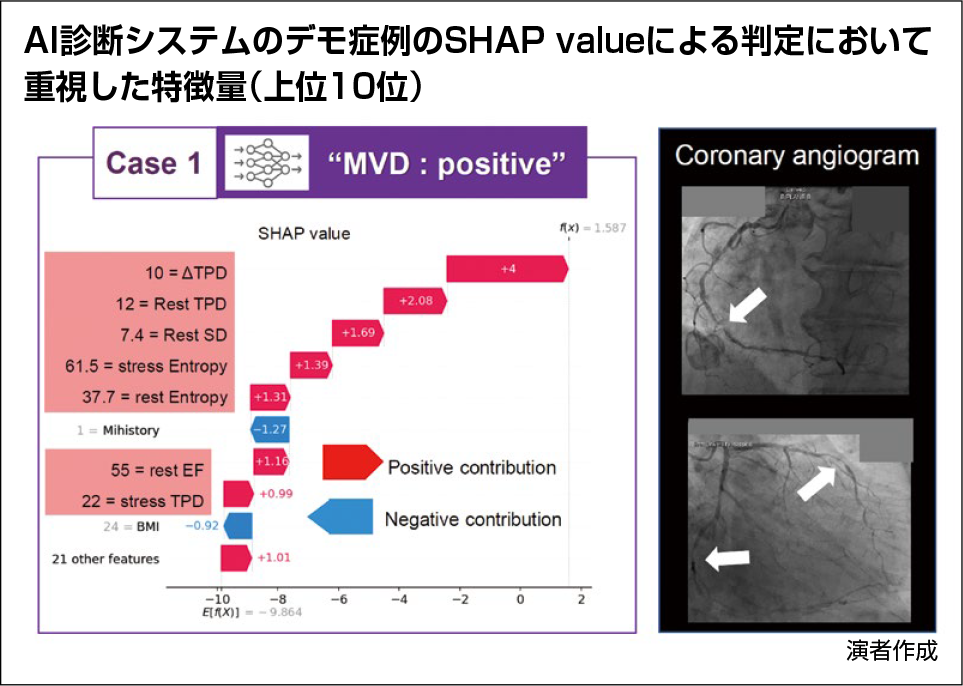
【図4】