4.心筋梗塞・心筋症
監修・症例提供
百瀬 満 先生
東京女子医科大学 画像診断学・核医学講座
EAPで心臓カテーテルを行い、LCX#13完全閉塞に対してPCIの既往あり。
今回、心電図検査で無症候性MI(前壁)が疑われた。
糖尿病で通院中。
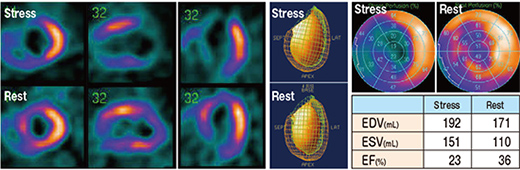
運動負荷心筋SPECTを施行したところ、LAD領域の梗塞と虚血、下壁に一過性心筋虚血を認めた( ![]() )。
)。
QGSではTID比1.12、一過性LVEFの低下(ー13%)を認め、SSS、SRS、SDS(全心筋の割合%)はそれぞれ42(62%)、12(18%)、30(44%)、CAGでは#7 99%、#3 100%の2枝病変と診断。
極めて高リスク患者であり、2ヵ月後にLADに対してPCIを施行。
無症候性OMIでは一般に梗塞関連冠動脈に高度狭窄が残存している。
同部位にviabilityがあるか、心筋虚血がどの程度あるかにより治療方針が異なる。
本例では#3、#7に高度狭窄があったが、梗塞や虚血のほとんどは#7の支配領域であり、同部位のみにPCIを施行。
その後6年間薬物療法のみで生存が確認されている。
40歳代から運動時にふらつきの症状があったが放置。
最近、運動後の眼前暗黒感が出現したために当院紹介受診。
心エコーでは非対称性中隔肥大を認めたが、心機能は正常。有意な左室流出路の圧較差は認めなかった。
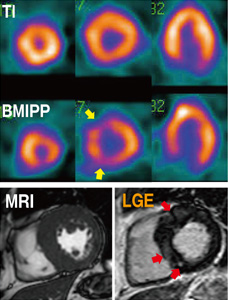
Tl/BMIPP 2核種同時心筋シンチグラフィの収集画像( ![]() 上)ではBMIPPで前壁中隔基部、後部中隔にBMIPPで軽度の集積低下を認め、Tlでは灌流低下は無いが、中隔と心尖部に集積亢進がある。
上)ではBMIPPで前壁中隔基部、後部中隔にBMIPPで軽度の集積低下を認め、Tlでは灌流低下は無いが、中隔と心尖部に集積亢進がある。
CMR(![]() 下)では中隔の心筋肥大とBMIPPとほぼ同じ領域にGd造影剤の遅延像(LGE)を認めた。
下)では中隔の心筋肥大とBMIPPとほぼ同じ領域にGd造影剤の遅延像(LGE)を認めた。
MRI上、EDV146mL、EF55%。
HCMのTl/BMIPP所見の特徴として、Tlの高集積(集積亢進)部位に、BMIPP集積が低下するミスマッチを認める。
また、MRIでは中隔の右室付着部でLGE陽性の頻度が高く、BMIPPの障害部位と一致することが多い。
本例は直ちに薬物療法が開始された。
Tl

BMIPP

心不全症状を機に近医で薬物療法を開始。
心エコーでびまん性の左室壁運動低下、高度左室拡大(左室拡張末期径/左室収縮末期径 83/74mm)を認めた。
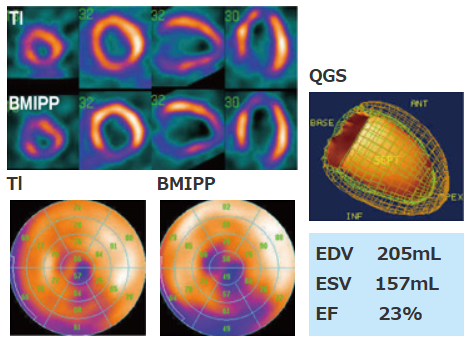
不全心の鑑別のため行われたTl/BMIPP 2核種同時心筋シンチグラフィ( ![]() )ではミスマッチはごく僅かで虚血は考えにくくCMRでもLGEを認めず。
)ではミスマッチはごく僅かで虚血は考えにくくCMRでもLGEを認めず。
CMRではEDV 355mL、ESV 322mL、LVEF 8%で著明な低心機能の所見( ![]() )あり。
)あり。
CAGでは有意狭窄はなく最終的にDCMと診断。MIBG( ![]() )では遅延像H/M比1.53で高度集積低下を認めた。
)では遅延像H/M比1.53で高度集積低下を認めた。
β遮断薬治療を開始し、左室機能の改善、MIBGのH/M比も著明に改善した(H/M比2.20)。
不全心の鑑別診断としてICMが挙げられるが、心サルコイドーシスなどの二次性心筋症の鑑別も必要である。
TlやBMIPP、CMRを用いた局所心筋障害精査の結果、本例はICMは除外されDCMと診断。
β遮断薬が著効し、MIBGでも集積改善を認めた。
糖尿病や心疾患の既往無し。
62歳より慢性糸球体腎炎による慢性腎不全で血液透析導入。
導入時は心エコーで左室機能正常。
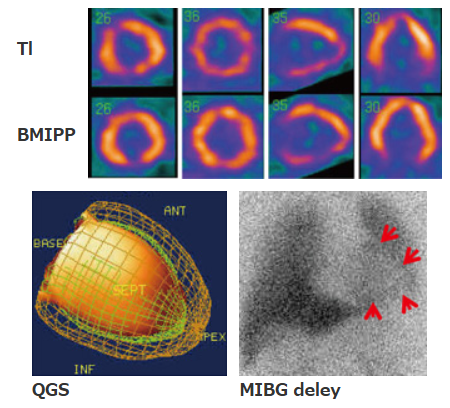
8年後心不全兆候あり、心エコーで高度の左室収縮不全を認めたため、Tl/BMIPP 2核種同時心筋シンチグラフィを施行。
BMIPPで心尖部および下後壁に高度集積低下を認め、血流代謝乖離を認めた。
QGSでは左室高度リモデリングを認めたため、ICMを疑い、CAGを施行。
LMT90%、 #7 90%、 #1 99%のLMT+2枝病変でBMIPPの異常部位とほぼ一致した。
虚血性心疾患の既往がなく、胸痛もないが心不全で入院する患者がICMと診断される場合がある。
DCMとの鑑別が必要となるが、ICMでは一般にBMIPPで局所集積低下を認め、Tlとミスマッチを認めることが多い。
しかし、二次性心筋症でも局所の欠損像がみられ鑑別困難な場合があり、MRIのLGEやCAGによる確認が必要である。
本例はその後、CABG(LIMA-LAD、SVG-PL-#4AV-#4PD)を施行された。