斎藤 史郎 先生
国立病院機構東京医療センター 泌尿器科
大橋 俊夫 先生
慶應義塾大学医学部 放射線治療科
門間 哲雄 先生
国立病院機構埼玉病院 泌尿器科
萬 篤憲 先生
国立病院機構東京医療センター 放射線科
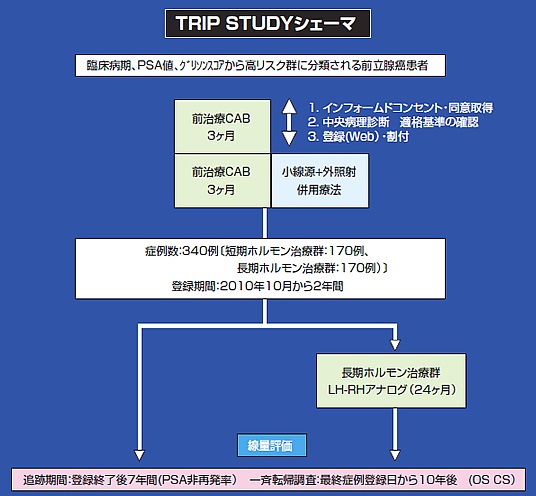
外照射併用シード療法
萬 篤憲 先生(国立病院機構東京医療センター 放射線科)
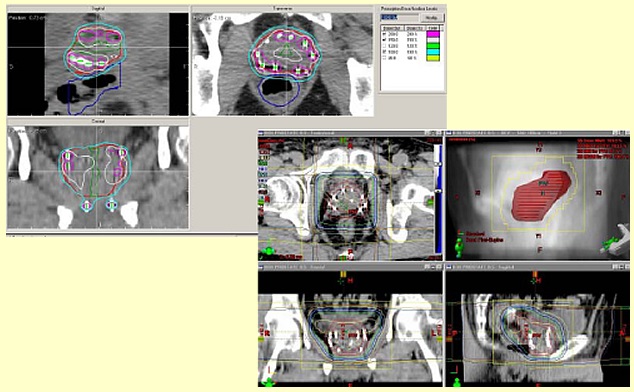
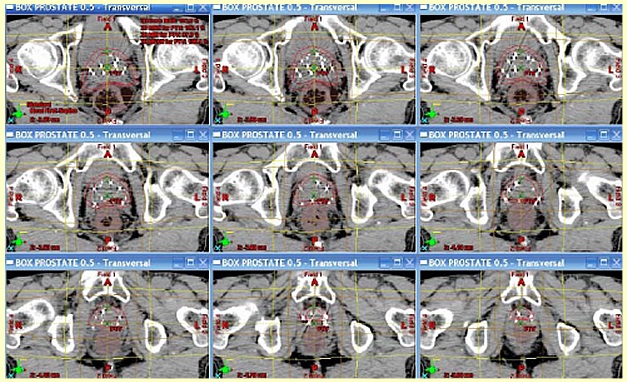
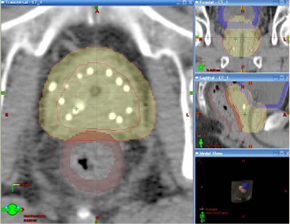
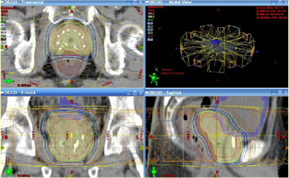
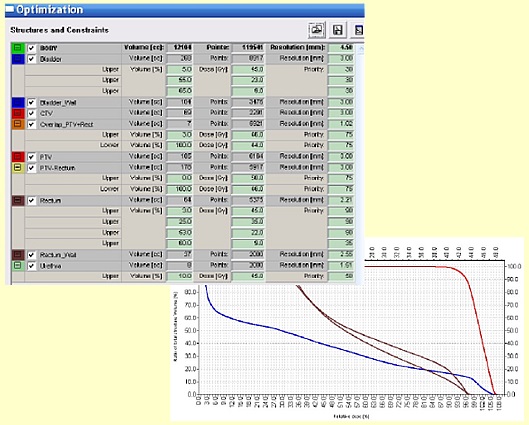
PTVと直腸壁の重なりの線量設定を行い、「PTV-直腸壁」には処方線量の95~107%が照射される。通常、PTVのD50が100%程度となる。
日本における先行施設の経験と失敗に学ぶ
主要先行多施設のデータ集積 東京医療センターのデータ解析
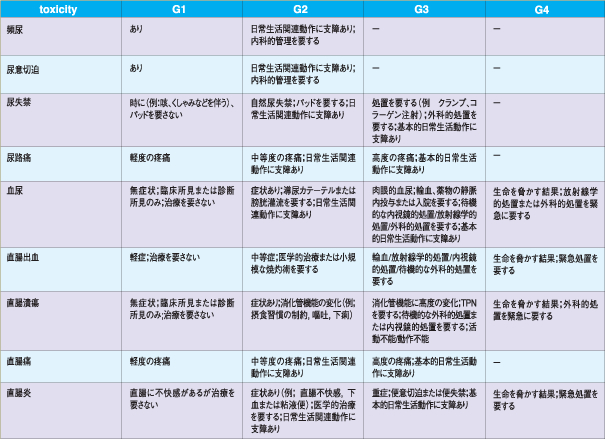
● 国内報告における有害事象の頻度
● 尿道の有害事象
● 線量増加はどの程度を目指すのか?
● 直腸の有害事象
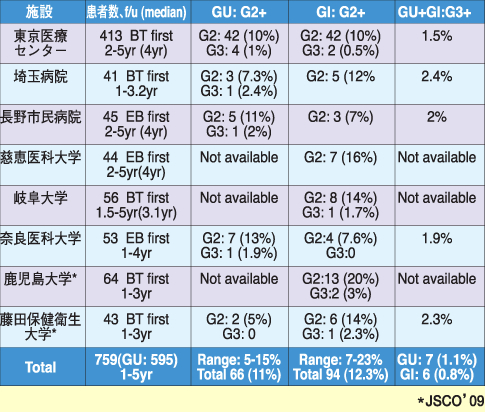
米国の主要施設から報告されている有害事象と比較して同等どの施設もシード単独と比較して直腸出血が多い
たとえ1例でも直腸瘻などG4が生じると、心身の負担は格段に重い
これまでに国内で報告されたシード関連の3例中2例の直腸瘻は直腸生検・痔の治療後に増悪
多施設前向研究では有害事象は単施設報告と比べ一般に増える
線量増加を目指す以上、有害事象は減らない。
G2+を極力減らし、G4を出さないアプローチが最重要課題である。
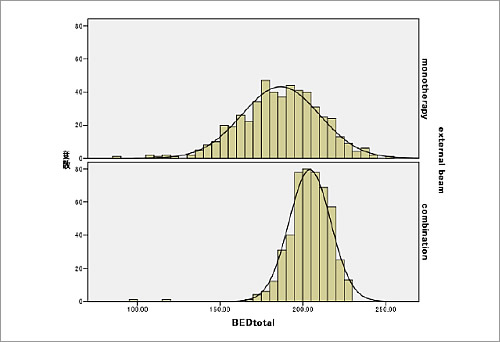
併用療法はシード単独と比較して明らかに安定してBED180~230Gy2(中央値204Gy2)を照射することが可能である。
BED240Gy2以上については当施設ではほとんど経験していない。その安全性について日本では確認されていないと考えられる。
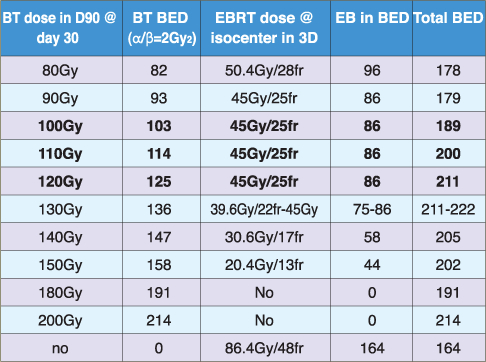
線量効果関係の実証は簡単ではなく、特に閾値の設定は困難
外照射単独ではBED170Gy2を超えることはかなり難しい
併用療法ではBED180~230Gy2を目指すことは比較的容易
Stoneらの報告はBED180Gy2以上で再発率も生検陰性率も頭打ちだがGS8~10の高リスクではBED220Gy2以上で再発率が低下すると報告
すでにある程度の安全性が示されている範囲を目標とすべき
計算上の理論を用いるのなら目標としてBEDで180~230Gy2は妥当
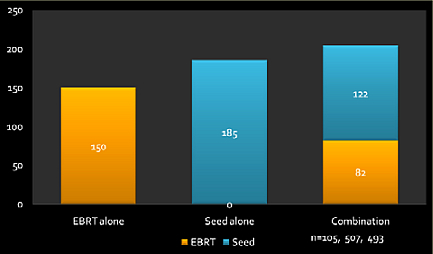
シードおよび併用療法は外照射に比べAcute G3(主に急性尿閉)が多い。
Acute G2+を左右するのは線量よりも前立腺肥大と高いIPSS。
併用療法は単独療法に比べLate G1+は増加するが、Late G3は増えない。
晩期毒性は治療後数年にわたり生じ、多くは1~3年後に一過性の尿道症状を生じる、いわゆるフレア現象。
多くは症状の説明で十分だが、G2が長引くときには薬物療法も検討。
尿道線量を計画通りに抑えれば重篤な毒性はまれであるが、G1~2の晩期毒性はしばしば生じる。 患者への丁寧な説明が重要
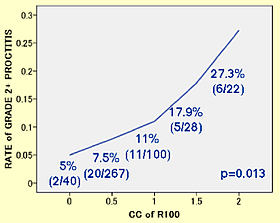
直腸晩期毒性はシードに比べ外照射や併用療法で明らかに多い。
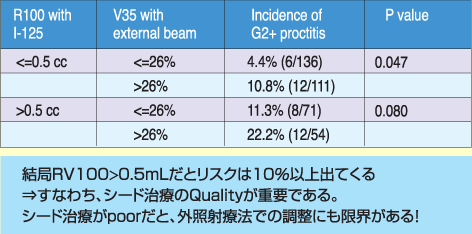
併用療法ではシード治療の術後RV100は0.5mL未満、RV150は0を目指す。
3次元照射、特にIMRTではシードによるDVHや線量分布を参考にして外照射の直腸線量を規定することが可能。
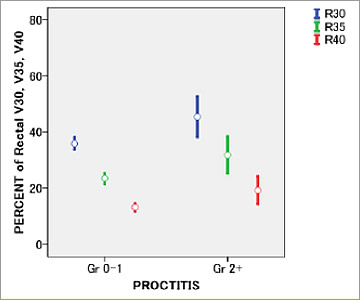
外照射においてRV30~40Gyを低く抑えることも有用。
シード先行の場合、直腸の体積線量因子をシードおよび外照射の両者で調節し、G2+毒性を減らすことが可能
TRIPの紹介