製品情報/特徴(特性)
禁忌
【禁忌】(次の患者には投与しないこと)
本剤の成分に対して過敏症の既往歴がある患者
【設定理由】
海外臨床試験において被験薬との関連が否定できない有害事象としてアナフィラキシー様反応が1 件報告されており、本剤の成分に対して過敏症の既往歴を有する患者では、過敏症反応を示す可能性がある。
効能又は効果
アルツハイマー型認知症が疑われる認知機能障害を有する患者の脳内アミロイドベータプラークの可視化。
効能又は効果に関連する使用上の注意
無症候者に対するアルツハイマー型認知症の発症前診断を目的として本剤を用いたPET 検査を実施しないこと
(アルツハイマー型認知症の発症予測に関する有用性は確立していない)。
用法及び用量
通常,本剤1バイアル(120~370MBq)を静脈内投与し、投与後60~120分に撮像を開始する。
用法及び用量に関連する使用上の注意
撮像時間は、投与量、撮像機器、データ収集条件、画像再構成のアルゴリズム及びパラメータ等を考慮して決定すること。
適切にバリデーションされたPET装置で撮像を行う場合、投与量185MBqにおける標準的な撮像時間は20 分間である。
組成・性状
本剤は、水性の注射剤で、フッ素-18をフルテメタモルの形で含む。
1バイアル(2mL)中
| フルテメタモル(18F) (検定日時において) 185MBq | |
| 添 加 物 | 日本薬局方無水エタノール 0.14mL, 日本薬局方ポリソルベート80 10mg, 等張化剤,pH調整剤2成分 |
| 外 観 pH 浸透圧比 |
無色~微黄色澄明の液 6.0~8.5 ―※ ※本剤の浸透圧はエタノールを含有することにより測定できない。 |
有効成分に関する理化学的知見
<一般的名称>
和名 : フルテメタモル(18F)、フルテメタモル(18F)注射液(放射性医薬品基準)
洋名 : flutemetamol(18F) (INN)
<化学名>
2-[3-[18F]fluoro-4-(methylamino)phenyl]-1,3-benzothiazol-6-ol(IUPAC法)
<分子式>
C14H1118FN2OS
<化学構造式>
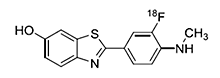
<核物理学的特性>
18Fとして
1.物理的半減期 : 109.8 分
2.主γ線エネルギー : 511keV
3. 減衰表
| 検定時間から(分) | MBq | 検定時間から(分) | MBq |
|---|---|---|---|
| -110 | 370 .5 | 10 | 173.7 |
| -100 | 347.8 | 20 | 163.1 |
| -90 | 326.5 | 30 | 153.1 |
| -80 | 306.6 | 40 | 143.7 |
| -70 | 287.8 | 50 | 134.9 |
| -60 | 270.2 | 60 | 126.7 |
| -50 | 253.7 | 70 | 118.9 |
| -40 | 238.1 | 80 | 111.6 |
| -30 | 223.6 | 90 | 104.8 |
| -20 | 209.9 | 100 | 98.4 |
| -10 | 197.1 | 110 | 92.4 |
| 0 | 185.0 | 120 | 86.7 |
| 130 | 81.4 | ||
| 140 | 76.4 |
注) 検定時間:規格単位を定める時間
-

11C-PiB(Pittsburgh Compound B)の基本骨格に着目し開発されたビザミル®静注
11C-PiBはアミロイドPET用薬剤として現在でも広く研究に用いられている。
本剤は11C-PiBの基本骨格であるPiB※のフッ素‐18標識化合物です。
※病理組織学的検査においてアミロイドの染色に使用されているチオフラビンTの構造に起源を有する化合物 -

脳内アミロイドβの有無をPET検査で可視化できます。
剖検でしか得られなかった病理学的情報が把握できます。
-
現行のアルツハイマー型認知症(AD)診断に本剤のPET検査が加わることで、AD診断精度向上に寄与することが期待されます。
アミロイドPET 診断結果が陰性
認知症の原因疾患がアルツハイマー病である可能性が低いと判断されます1)。アミロイドPET 診断結果が陽性
アミロイドβはAD以外の認知症でも認められるため、認知症の原因疾患の判断は、臨床症状や他の検査所見と合わせて行う必要があります。しかし これらを総合的に判断したときに、ADであることの確信度が増すことが期待できます1)。 -
用法・用量に幅があります。
患者様の状態やPET装置のデータ収集条件および画像再構成条件に応じて「投与量」「撮像開始時間」「撮像時間」を以下の範囲で調節できます。
※検定日時において185MBq有効期間 : 検定日時から68分 投与量 : 本剤1バイアル (120~370MBq)※ 撮像開始時間 : 投与後60~120分 撮像時間 : 120MBq投与時 30分
185MBq投与時 20分
370MBq投与時 10分
用法及び用量に関連する使用上の注意を参照 -
カラー画像による読影が推奨されています。
橋(pons)を最高輝度の約90%に調整したカラー画像(Sokoloff又はrainbow)で読影・判定します。
-
副作用
<国内臨床試験及び日本人を対象とした国際共同臨床試験>
92 例中2 例(2%)に4 件の副作用が認められた。副作用は1 例で心窩部不快感、潮紅及び高血圧、もう1 例で頭痛であった。
<海外臨床試験>
739 例中44 例(6%)で92 件の副作用が認められた。主な副作用は、潮紅16 件(2%)及び悪心8 件(1%)であった。
重大な副作用
アナフィラキシー(0.1%):アナフィラキシーを起こすことがあるので問診を十分に行い、投与後は十分に観察し、顔面潮紅、呼吸困難及び胸部圧迫感等の症状が認められた場合には適切な処置を行うこと。
引用文献1)承認時評価資料
